Простой способ очищения ржавчины
Конечно, ни один уважающий себя мастер просто так не бросит свои инструменты на произвол судьбы под открытым небом. Но кому из нас не случалось обнаружить давным – давно позабытый рубанок, топор или стамеску где – нибудь в дальнем углу сарая или в гараже. Пролежав всего одну зиму в сыром месте, они обязательно покрываются толстым слоем ржавчины, удалить которую не так то просто. Шкурка и другие абразивные материалы помогают лишь там, где ржавчина «въелась» не слишком глубоко. Там же, где она внедрилась основательно, снять ржавчину абразивными инструментами удается только в месте с изрядным слоем «живого металла».
Археологам известен способ удаления ржавчины с поверхности любых железных предметов, которые пролежали в земле десятки и сотни лет. Причем очень бережно, когда сами образцы остаются в целости и сохранности, не подвергаясь никаким повреждениям. Суть этого способа – в электрохимическом преобразовании ржавчины в щелочном растворе. При этом под воздействием электрического тока плотный слой оксидов железа (ржавчина) превращается в черный рыхлый порошок, который легко удаляется простым промыванием струей воды.
Рис.1
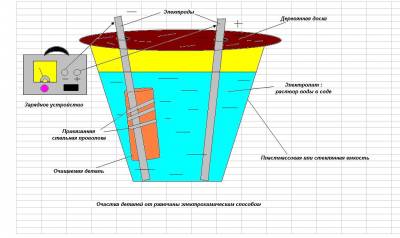
Сам себе процесс электрохимического преобразования достаточно прост и безопасен, поэтому его вполне можно реализовать в домашних условиях. Для этого понадобится источник постоянного тока напряжением 12 – 14 В, например, зарядное устройство для автомобильных аккумуляторов. Подойдет практически любое, в котором предусмотрена плавная регулировка тока в диапазоне от 0 до 2 А. Еще потребуется большая емкость из неэлектропроводящего материала, в качестве которого можно использовать любое пластмассовое ведро объемом 10 – 15 л или нечто подобное. Для проведения электрохимического процесса в растворе придется сделать два электрода – анод и катод. Оба они должны быть обязательно стальными. Проще всего изготовить их из прутков арматуры диаметром 10 – 15 мм и длиной 0,5 м.
Электролитом для проведения процесса преобразования ржавчины служит раствор каустической соды (Na2CO2, проще говоря «Сода для стирки») с концентрацией около 25 г/л. Чтобы приготовить его, нужно растворить примерно 250 г соды в ведре обычной холодной воды.
Покрытый ржавчиной инструмент крепко привязывают к концу одного из электродов (катоду) мягкой стальной проволокой (медную проволоку использовать нельзя). Предварительно нужно обязательно снять с инструмента все медные, латунные, алюминиевые, оцинкованные и деревянные детали. Подвергать электрохимической обработке можно только стальные детали. Оба электрода – и катод с деталью, и анод опускают в емкость с раствором до самого дна, раздвинув их подальше друг от друга, и фиксируют в таком положении, надев на верхние концы прутков – электродов брусок или доску с двумя отверстиями, как показано на рисунке.
Выводы зарядного устройства подключают к электродам: минусовой – к катоду, а плюсовой – к аноду. Включают зарядное устройство в сеть и регулятором выставляют ток примерно 2 А. Если все сделано правильно, то в растворе должны почти сразу появится всплывающие пузырьки газа, как в стакане с газировкой. Это верный признак того, что все идет как надо. Из – за выделения довольно большого количества газов весь процесс нужно проводить на открытом воздухе или в очень хорошо проветриваемом помещении. Никакой опасности для здоровья эти газы не представляют, в основном это кислород и водород, но запах в закрытом помещении будет не очень приятный.
Длится процесс преобразования ржавчины не долго – минут 30 – 35. Когда вся ржавчина превратится в черный порошок, ток можно отключить и извлечь из раствора очищаемые детали. Их нужно сразу же промыть под струей водопроводной воды, а затем ополоснуть кипяченой. Оставлять надолго очищенные детали и инструменты во влажном состоянии нельзя. Лучше сразу обтереть их сначала сухой, а потом слегка промасленной ветошью.
Журнал «Сам»
4№, 2005 г